Азотоводородна киселина
Азотоводородната киселина, HN3, е едноосновна безкислородна киселина на азота. Представлява силно експлозивна безцветна течност. Дава соли, наречени азиди.
Строеж
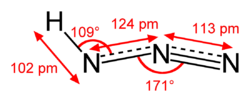
В молекулата на HN3 азотният атом, свързан с водорода, образува две σ-връзки и една резонансна π-връзка, резултат от sp2-хибридизация. Централният азотен атом (с формален заряд +1) отдава електрон на третия азотен атом (с формален заряд −1). Трите азотни атома са подредени почти в права линия. Между тях се образуват двойни π-връзки и единични σ-връзки.
Физични свойства
Азотоводородната киселина е безцветна летлива течност, кипяща при 37 °C.[1] Сублимира лесно. Има неприятна миризма и е отровна. Безводната киселина е силно експлозивна.
Химични свойства
Водният разтвор на азотоводородната киселина е слаба киселина със сила, близка до оцетната:
Азотоводородната киселина може да реагира с азиден йон до хидрогеназиден йон – N3HNШаблон:Индекси.
Във воден разтвор търпи бавно диспропорциониране:[1]
HN3 е силен окислител. Разтваря Zn, Fe, Mn и Cu без отделяне на H2:
Йодът и Ce(IV) соли я редуцират до N2.
Смес от солна и азотоводородна киселина действа като царска вода и може да разтвори златото и другите благородни метали. Причината е полученият хлор при реакцията между двете киселини, при която HN3 е окислител:
При реакция с много силни основи азотоводородната киселина се държи като основа:
Азиди
Шаблон:Основна Солите на азотоводородната киселина се наричат азиди и по разтворимост във вода приличат на хлоридите.[1] Азидите на алкалните и алкалоземните метали са силно разтворими. При бавно загряване те са устойчиви до стапянето си. Освен CsN3, те се топят с разлагане:[2]
Най-използваната сол е натриевият азид, който се получава при пропускане на диазотен оксид в амонячен разтвор на натрий или при взаимодействие на същия оксид с натриев амид:
Азидите на тежките метали (AgN3, Hg(N3)2, Pb(N3)2) са слабо разтворими във вода. Те се получават от водните разтвори на солите на тези метали при утаяване с натриев азид. Всички те са избухливи вещества, които се разлагат при удар и нагряване.
Получаване
Азотоводородната киселина за първи път е получена от окисление на хидразин с азотиста киселина:[2]
Азотоводородната киселина се получава от алкални азиди и по-силна киселина, например концентрирана сярна киселина:
HN3 се изолира от сместа с вакуумна дестилация.[2]